转自:中国科技网
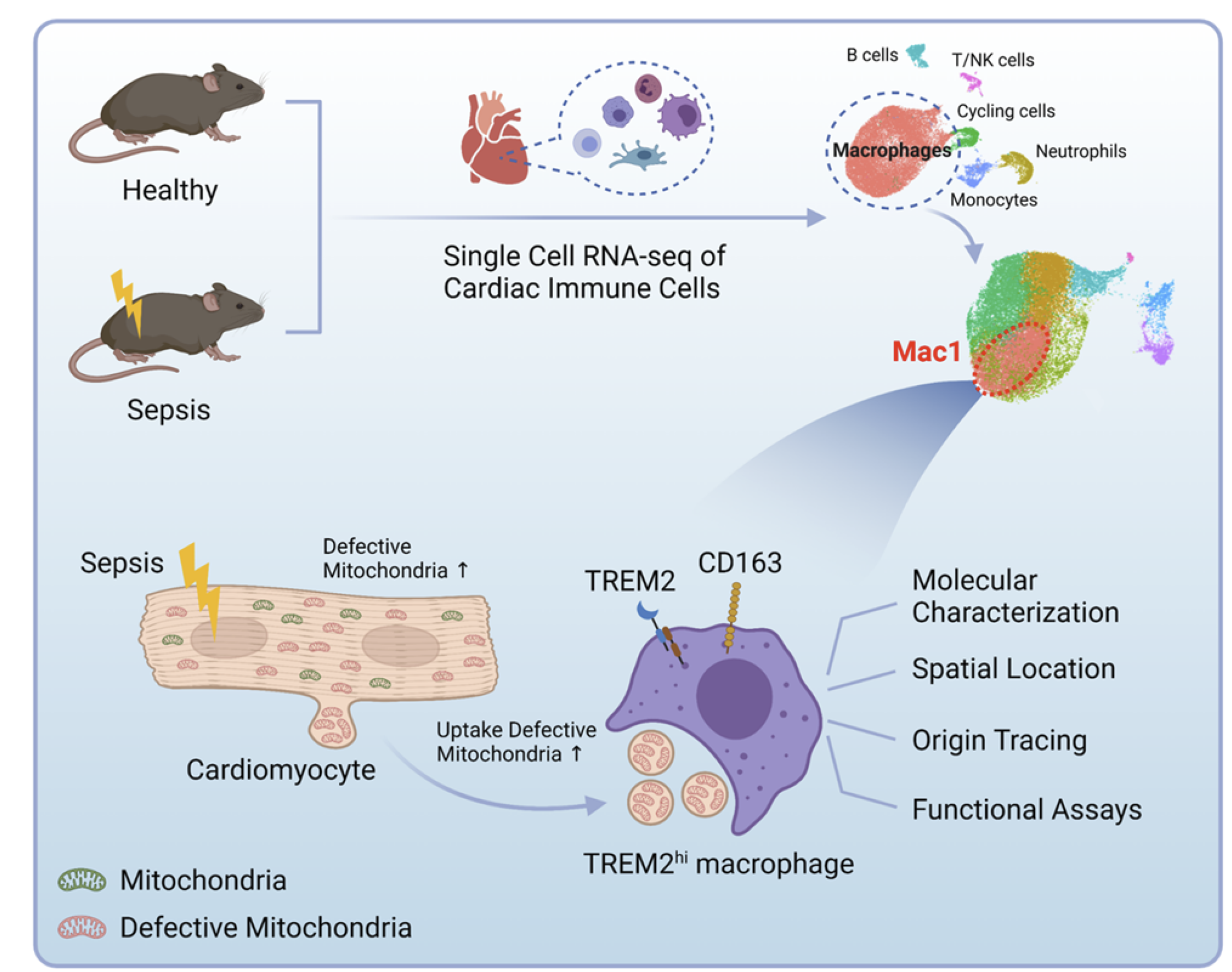 脓毒症心脏常驻巨噬细胞调控心肌细胞线粒体平衡的机制。科研团队供图
脓毒症心脏常驻巨噬细胞调控心肌细胞线粒体平衡的机制。科研团队供图洪恒飞 科技日报记者 江耘
近日,国际期刊《自然·代谢》刊登了浙江大学医学院方向明教授团队的最新成果。该团队从心脏常驻巨噬细胞中发现了影响脓毒症心功能恢复的关键细胞亚群,并阐明其作用机制,提出了具有临床前景的脓毒症心肌病治疗策略。
脓毒症是指由感染引发机体免疫紊乱,造成组织器官出现不同程度的损伤。其中,心脏的收缩舒张泵功能一旦受损,将引发脓毒症心肌病,各器官有效灌注难以维持,患者预后会迅速恶化。目前,脓毒症心肌病缺乏有效的治疗策略,危重患者需要依赖体外膜肺氧合机、人工心移植来短期维持生命功能。
“线粒体功能障碍是脓毒症心肌病期间的一个关键特征。健康的免疫微环境在心肌细胞的线粒体稳态和代谢功能维持方面,起着相当重要的作用。”科研人员发现,健康的心肌细胞有其独特的线粒体质量控制机制——由心肌细胞释放损伤线粒体形成的细胞外囊泡exophers,会被巨噬细胞吞噬并清除。
在免疫细胞中,组织驻留巨噬细胞作为一种常驻于组织中且具有一定自我更新能力的固有免疫细胞,是健康心脏的重要组成部分,会对感染做出早期反应。在患脓毒症心肌病的实验动物体内,研究团队首次发现了一群高表达髓系细胞触发受体2(TREM2)的心脏巨噬细胞亚群,数目会先减后增。这一动态变化与患脓毒症后存活的实验动物“心脏功能明显受损,随后逐渐好转”的病情变化对应。
对此,研究团队应用大量遗传模型和实验方法加以验证,发现TREM2基因敲除或高表达TREM2巨噬细胞缺失会导致心脏功能障碍加剧,心包内同种异体移植高表达TREM2巨噬细胞可治疗脓毒症心功能障碍,说明高表达TREM2的心脏常驻巨噬细胞在脓毒症心肌病中发挥重要作用。
研究团队发现,患脓毒症时,TREM2高表达的巨噬细胞是心脏的“代谢卫士”,其数量和比例的减少将会导致心肌中的exophers清除障碍、损伤线粒体堆积。与其他巨噬细胞亚群相比,心肌细胞释放的含有损伤线粒体的exophers会优先被高表达TREM2的巨噬细胞摄取。
科研人员表示,基于高表达TREM2的巨噬细胞的特殊功能,期待临床上能开发出针对脓毒症心肌病的多种治疗策略。



